| 対象疾患 | 治療ライン | 研究の相 | 主要評価項目 | 実施地域 | 日本の参加 |
|---|---|---|---|---|---|
| 胃癌 | 一次治療 | 第3相 | 全生存期間 | 国内 | あり |
試験名 :JCOG9205
レジメン:5-FU単剤 vs 5-FU+シスプラチン vs UFT+マイトマイシン
登録期間:1992年9月〜1997年3月
背景
本試験の立案当時、切除不能進行・再発胃癌においては、いくつかの無作為化比較試験でBest supportive care(BSC)と比較し、5-FUベースのレジメンで生存期間の延長効果が報告されてはいるものの、標準治療は確立されていなかった。本試験の開始までに日本臨床腫瘍研究グループ(JCOG)で実施されたテガフール+マイトマイシン療法とUFT+マイトマイシン療法(UFTM)の無作為化比較試験では、UFTM療法で高い奏効割合を示したが、生存期間は両群間で相違がなかった。その後に行われた3つのプラチナ併用療法の臨床試験(ドキソルビシン+シスプラチン、エトポシド+ドキソルビシン+シスプラチン(EAP)、5-FU+シスプラチン(FP))では、EAP療法で高い奏効割合と良好な生存期間を示したものの、10%近い治療関連死亡を来したため、その後の臨床試験には許容できないと判断された。一方、FP療法とドキソルビシン+シスプラチン療法に関しては、両者の治療効果に差はなく、同等な結果であった。
これらの試験の終了後、標準治療確立のために5-FU単剤療法と5-FU+ドキソルビシン+マイトマイシン併用療法を比較する無作為化比較試験を実施したが、3剤併用療法にて生存期間の延長は示せなかった。
これらの臨床試験の結果より、切除不能進行・再発胃癌の標準治療を確立すべく、5-FU単剤療法を対照群として、世界で広く使われているFP療法と 日本国内で広く使われているUFTM療法の有効性、安全性を検証する第3相試験が実施された。
これらの試験の終了後、標準治療確立のために5-FU単剤療法と5-FU+ドキソルビシン+マイトマイシン併用療法を比較する無作為化比較試験を実施したが、3剤併用療法にて生存期間の延長は示せなかった。
これらの臨床試験の結果より、切除不能進行・再発胃癌の標準治療を確立すべく、5-FU単剤療法を対照群として、世界で広く使われているFP療法と 日本国内で広く使われているUFTM療法の有効性、安全性を検証する第3相試験が実施された。
シェーマ
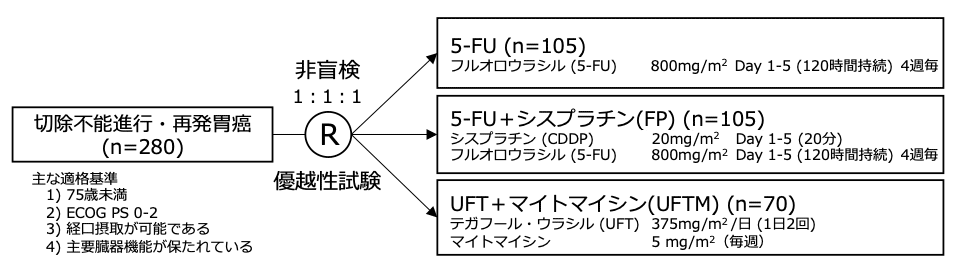
統計学的事項
主要評価項目:全生存期間
症例数の計算は過去の第II相試験における6ヶ月および12ヶ月の生存データに基づいて計算された。5-FU単独群と比較して、FP群とUFTM群の全生存期間が、対照群を上回るかどうかを検証する優越性試験として設計され、検出力80%、両側α=0.05として、309人(各群103人)の登録が必要と設定された。本試験の登録期間は3年、最終症例登録後1年の追跡を行うこととして計画された。
試験結果:
- 試験開始後3年で行われた初回の中間解析にて、UFTM群の生存期間が5-FU群と比較して有意に劣っており、UFTM群の登録が中止された。
- 1992年9月から1997年3月までの間に31施設から280例が登録された(5-FU群 105例、FP群 105例、UFTM群 70例)。
- 5-FU群の1例、FP群の3例、UFTM群の3例は実際の治療を受けておらず、安全性解析から除外された。
- 平均観察期間は5-FU群 8.9ヶ月、FP群 10.1ヶ月、UFTM群 7.6ヶ月であった。
- 患者背景は3群間で概ねバランスがとれていた。253例(90%)がECOG PS 0-1であり、248(89%)例が測定可能病変を有していた。また77例(28%)が登録前に胃切除術を受けていた。
1. 全生存期間(主要評価項目)
| 中央値 | 95%信頼区間 | 1年生存割合 | 2年生存割合 | 5-FU vs. FP p=0.34 5-FU vs UFTM p=0.11 |
|
| 5-FU | 7.1ヶ月 | 5.8-8.2 | 28% | 7% | |
| FP | 7.3ヶ月 | 6.0-9.7 | 29% | 7% | |
| UFTM | 6.0ヶ月 | 4.6-7.4 | 16% | 4% |
2. 無増悪生存期間
| 中央値 | 95%信頼区間 | 5-FU vs. FP p<0.001 |
|
| 5-FU | 1.9ヶ月 | 1.3-2.7 | |
| FP | 3.9ヶ月 | 3.1-4.8 | |
| UFTM | 2.4ヶ月 | 1.3-3.2 |
3. 奏効割合
| 奏効割合 | 95%信頼区間 | 5-FU vs. FP p<0.001 |
|
| 5-FU | 11.4% | 6.0-19.1 | |
| FP | 34.3% | 25.3-44.2 | |
| UFTM | 8.6% | 3.2-17.7 |
4. 投与状況/後治療
- 投与サイクル中央値(範囲)
5-FU:2サイクル(1-13)
FP:3サイクル(1-11)
UFTM(マイトマイシンの投与回数):6回(1-23) - 最も高頻度のプロトコール治療中止理由は病勢進行で次に高頻度なのが有害事象であった。
- 有害事象中止は5-FU群と比較して、FP群・UFTM群でより高頻度であった。
- 患者拒否による中止は5-FU群(7%)・UFTM群(7%)と比較して、FP群(25%)でより高頻度であった。
- 5-FU群 60例(57%)、FP群 55例(52%)、UFTM群 34例(49%)で二次化学療法が実施された。
- 3群合わせて最も頻用された(約40%)二次化学療法レジメンはMTX+5-FU、続いてシスプラチン併用レジメン(FPまたはイリノテカン+シスプラチン)であった。
5. 有害事象(%)
| 5-FU (n=104) | FP (n=102) | UFTM (n=67) | P | ||||
|---|---|---|---|---|---|---|---|
| 全Grade | Grade 3以上 | 全Grade | Grade 3以上 | 全Grade | Grade 3以上 | ||
| 白血球減少 | 22.5 | 1.0 | 82.4 | 26.5 | 64.2 | 25.4 | <0.001 |
| 好中球数減少 | 23.8 | 5.0 | 84.7 | 53.1 | 60.7 | 37.7 | <0.001 |
| 貧血 | 71.6 | 9.8 | 90.2 | 25.5 | 74.6 | 14.9 | 0.22 |
| 血小板数減少 | 4.0 | 2.0 | 44.1 | 17.6 | 55.2 | 29.9 | <0.001 |
| 血中ビリルビン増加 | 17.8 | 5.9 | 26.5 | 7.8 | 35.8 | 11.9 | 0.17 |
| クレアチニン増加 | 15.7 | 1.0 | 35.3 | 2.0 | 16.4 | 0 | 0.65 |
| 低ナトリウム血症 | 55.4 | 2.0 | 90.0 | 5.9 | 53.0 | 3.0 | 0.59 |
| 悪心/嘔吐 | 58.4 | 5.0 | 86.1 | 7.9 | 75.8 | 10.6 | 0.17 |
| 下痢 | 20.8 | 0 | 33.7 | 3.0 | 27.3 | 0 | 0.77 |
| 粘膜炎 | 32.7 | 1.0 | 42.0 | 6.0 | 16.7 | 1.5 | 0.63 |
| 神経障害:感覚性 | 4.0 | 0 | 10.9 | 1.0 | 7.6 | 0 | 0.87 |
| 発熱 | 20.8 | 2.0 | 32.0 | 2.0 | 19.7 | 0 | 0.34 |
| 早期死亡割合 | 9.5 | 6.7 | 32.0 | - | |||
| 治療関連死亡 | 1.0 | 3.8 | 1.4 | - | |||
- FP群・UFTM群における重篤な血液学的有害事象の頻度は5-FU群に比して有意に高かった。
- 3群で最も高頻度な非血液学的有害事象は悪心/嘔吐であり、Grade 2-3の悪心/嘔吐は5-FU群(16%)に比して、FP群(51%)、UFTM群(41%)で高頻度であった。
- 5-FU群・FP群における口内炎の頻度は、UFTM群より高頻度であった。
結語
UFTM療法とFP療法の試験治療は、5-FU単剤療法と比較し、全生存期間の有意な延長が認められなかった。以上より、進行胃癌における次の臨床試験試験の標準治療は、引き続き、5-FU単剤療法で継続される予定である。
執筆:独立行政法人国立病院機構 大阪医療センター 消化器内科 医師 長谷川 裕子 先生
監修:北海道大学病院 消化器内科 助教 結城 敏志 先生
監修:北海道大学病院 消化器内科 助教 結城 敏志 先生